
2020上半年,受到新冠疫情影响,各行各业都在面临着不同情况之下的挑战。对于药企而言,复工延迟、运输受阻、物流及人员流动、医院就诊大幅受限,每个挑战都是个不小的难题。
然而,对于作为国内领先的药企三生制药(1530.HK)则是在挑战下稳健前行,乘风破浪。其核心在研产品赛普汀®作为国产首个抗HER2单抗新药上市,分拆三生国健成功登陆科创板。那么,公司在疫情之下的业绩如何?
疫情之下的三生制药:2020上半年归母净利同比增加118.64%
根据公司公告显示,2020上半年,三生制药营业收入26.95亿元,同比增长2.0%;毛利22.17亿元,同比增长1.5%;毛利率82.7%;归母净利润7.02亿元,同比增长118.6%;EBITDA为10.03亿元,同比增长70.7%;经营业务产生现金流量净额7.08亿元,同比增长1.2%;杠杆比率(不包括债券)由2019年同期的13.7%,下降至4.1%。
图表一:公司财务状况
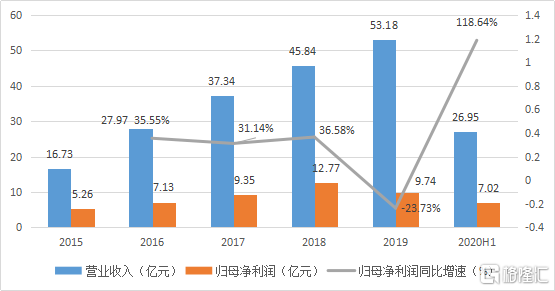
数据来源:公司资料,整理
受到外部环境影响之下还能拥有超过118%的归母净利润增速,这在业内处于什么水平?可以说是非常高的水平了。根据WIND数据统计显示,在A股中(港股存在会计准则,年报时间披露不一致等情况,所以选择A股)选取按照WIND行业划分的医药行业中,筛选今年中报披露(由于目前有些企业暂未露今年中报,可能存在遗漏)归母净利润大于等于7亿元,同比增速超于或等于118%,并且营业收入增速大于等于2%的公司,共计三家,分别是:达安基因(002030.SZ)、奥美医疗(002950.SZ)以及振德医疗(603301.SH),主营业务均与抗疫物资相关,处于新冠疫情正面影响企业,业绩拥有高增长性。
图表二:条件选股
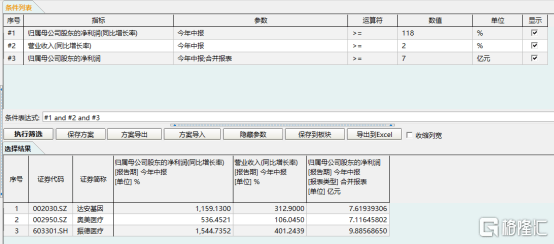
数据来源:WIND,整理
业绩爆发背后:核心产品铸造护城河
与抗疫物资相关来获得业绩高速增长不同,三生制药能够拥有高速增长的归母净利润,背后离不开公司一直以来的发展战略:发挥集“研发+生产+销售+对外合作”的体系化竞争优势,实现收入和利润的各项指标稳健增长。
三生制药拥有多款核心产品,疫情之下核心产品收入总体稳定,多款独家产品正在铸就公司稳固的护城河。
其中,2020上半年特比澳收入13.75亿元,益赛普收入3.31亿元,益比奥/赛博尔收入4.62亿元,蔓迪收入1.29亿元,其他核心产品收入3.87亿元。四款产品在2015年至2019年销售收入年复合增长率分别为39.8%,7.96%,0.75%,79.65%以及28.04%,收入占比分别为51%,12.3%,17.1%,4.8%以及14.8%。
图表三:公司核心产品收入
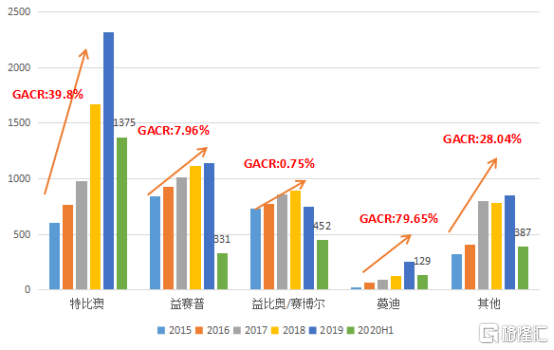
数据来源:公司公告,整理
公司自主研发的特比澳,是全球唯一商业化的rhTPO产品,已获得国家药监局批准两种适应症:之类化疗引起的血小板适应症(CIT)以及之类免疫性血小板适应症(ITP)。自2019年被纳入新医保目录乙类药以来,特比澳市场份额进一步提升。2020上半年特比澳收入13.75亿元,同比增长15.16%。
在最新研发上,公司已经开始进行特比澳用于儿童ITP的临床III期试验的患者招募工作,用于治疗血小板减少风险的肝功能障碍患者在围手术期的动员的临床I期试验已完成,并计划近期开展临床II期试验。目前,特比澳已经获得包括中国在内的9个国家批准,包括乌克兰、菲律宾及泰国。据国信证券预计,未来特比澳将成为销售额过30亿元的大品种。
益赛普是中国首个上市的肿瘤坏死因子α抑制剂,用于治疗类风湿性关节炎,强直性脊柱炎和银屑病,新版医保目录已将三种适应症囊括其中。2020上半年,益赛普收入3.31亿元,中国市场份额54.5%,涵盖中国内地超过3000家医院,其中超过1500家三甲医院。
在最新研发上,公司的预充式益赛普水针剂已完成临床III期试验,并已向国家药监局申请生产批件并获得受理。目前,益赛普已经获得包括中国在内的16家国家批准,包括哥伦比亚、泰国、菲律宾以及巴基斯坦。伴随着新医保中新增银屑病适应症,公司也将继续下沉市场发展,益赛普有望从当前5%-9%的市场渗透率进一步提升。
益比奥和赛博尔是国内唯一一家获得三种适应症的促红素品牌,自2002年起一直处于rhEPO市场支配性领导地位,2019年新医保新增非骨髓恶性肿瘤化疗引起的贫血适应症,中标价格稳定。2020上半年,益比奥和赛博尔合计收入4.62亿元,同比增长2.3%。在最新研发上,公司已经就第二代长效产品开始进入临床II试验,未来将会继续保持快速稳定的增长趋势。
蔓迪(米诺地尔町)是唯一一种受到《中国雄激素性秃发诊疗指南》推荐的外用药物,2015年至2019年收入年复合增长率达到79.65%,伴随着电商渠道成为产品销售新增长点,2020上半年收入1.29亿元,同比增长19.44%,预计未来三年后销售额有望超10亿元。
未来看点:新药上市增添助力,体系化竞争优势显著
那么,除了公司传统的核心产品增长强劲外,公司未来还有哪些看点值得关注?
一方面,公司在研产品陆续获批上市走向商业化,为公司发展增添助力。另一方面,产品商业化背后所需的生产销售以及对外合作,也将辅助公司在体系化竞争中脱颖而出。
赛普汀®:国产首个抗HER2单抗新药上市
2020年6月19日,公司自主研发的注射用伊尼妥单抗(商品名:赛普汀®)正式获得国家药监局批准,用于和化疗联合治疗HER2阳性的转移性乳腺癌。7月1日,赛普汀®已分别在北京、国家癌症中心/中国医学科学院肿瘤医院、江苏、安徽、山东和浙江神速开出首张处方,成为我国首个获批的自主研发抗HER2单抗。
根据国家癌症中心2019年公布的数据统计显示,乳腺癌发病率已经成为女性恶性肿瘤第一位。在众多乳腺癌患者中,大约有25%的患者表现为HER2阳性。根据Frost&Sullivan数据显示,中国抗HER2单抗药物市场从2015年16亿元增长至2019年已经达到66亿元,年复合增长率为42.3%。随着乳腺癌新药的加速上市,更多新药和生物类似药的可及性提高,抗HER2单抗药物市场未来将快速发展,预计在2024年达到约128亿元的市场规模,年复合增长 14.3%。
从竞争格局上来看,公司的赛普汀®为首家国产抗HER2单抗,产品完全能覆盖大部分晚期方案。今年上半年公司主要采取赠药策略,实行买三赠三,预计下半年和未来将会根据市场采取多样化政策,并积极争取进入医保。
图表四:国内抗HER2单抗药物市场规模及预测
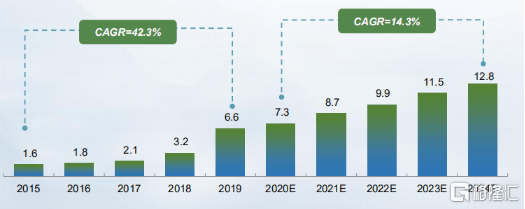
数据来源:公司资料,整理 单位:十亿元人民币
创新研发持续落地,成未来发展重要引擎
截止2020年6月30日,公司共计在研产品32项,其中22项为国家新药开发。按照治疗领域划分来看,公司共计拥有11项肿瘤科在研产品;12项在研产品为自身免疫疾病(包括RA),及其他疾病,包括顽固性痛风及眼科疾病(如AMD);6项肾科在研产品;2项代谢类在研产品,目标为2型糖尿病;及一项皮肤科在研产品。
图表五:在研产品管线
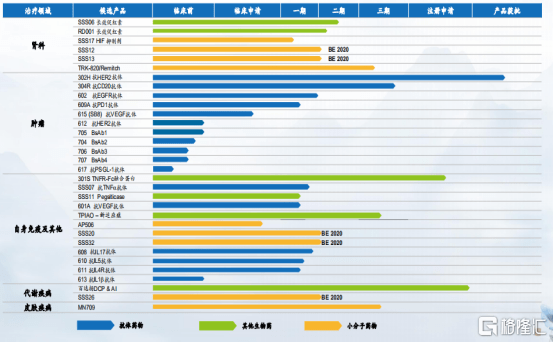
数据来源:公司资料,整理
在业绩期内,公司在研发进程上获得多项进展。其中,611(抗IL-4Ra抗体)临床试验申请获得FDA批准,并获得NMPA受理;610(抗IL-5抗体)获得NMPA临床试验批准,并开始一期临床入组;609A(抗PD-1抗体)美国一期临床试验完成患者入组,并开始中国患者入组;608(抗IL-17A抗体)完成一期临床试验者入组,正计划二期临床试验;601A(抗VEGF抗体)完成AMD一期病人入组,DME一期入组进展顺利;TRK-820(Remitch)完成三期桥接临床试验第一阶段入组;SSS17(HIF-17)开始一期临床试验患者入组;MN709(米诺地尔泡沫剂)开始三期临床试验患者入组;SSS06(长效促红素)多个一期完成开始二期患者入组。
而在未来三年(2020年至2022年),公司的研发产品也将持续落地,迎来收获期。包括2款新药上市(赛普汀®已上市),10-15个新的抗体和双抗的IND申报(中美双报),14项上市申请提交,启动6项注册性试验,6项临床II期到临床III期试验以及6项临床I期到临床II期试验。
图表六:2020-2022年研发产品线展望
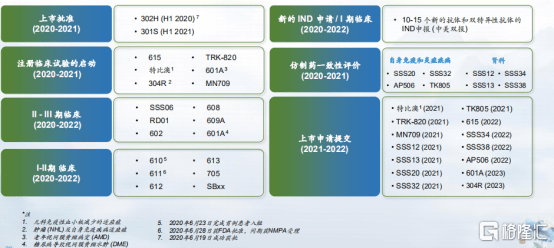
数据来源:公司资料,整理
不仅手握多项在研产品临近商业化,公司还在布局多个成熟热门靶点并且进行广泛覆盖。具体来看,公司囊括了包括HER2、PD-1、EGFR、VEGF、PSGL-1等市场空间较大的重点成熟靶点。另外,公司还在聚焦在研发下一代生物疗法,包括巨噬细胞靶向免疫疗法、编程CAR-T细胞疗法、双特异性抗体、多特异性抗体以及其他新型肿瘤免疫计划,每一项都是业内超前的研发技术,将为公司未来自主研发提供核心竞争力。
具备临床与销售快速迭代能力,对外合作持续强劲
对标海外药企,龙头企业的核心资产和核心竞争力在于,临床与销售快速迭代能力。而在中国,已经明确具备临床与销售快速迭代的药企实际上非常稀缺,其要求产品数量多,且有科室学术推广力量,具备大单品。单一大单品公司、仿制药或普药公司、销售简单粗暴不需要学术推广公司都不满足。
那么对于三生制药,是否满足临床与销售快速迭代能力呢?答案是有的。公司在研产品数量已经达到32项,其中核心产品特比澳更是在2019年样本医院创新药中销售金额TOP10的重磅产品。
而对于销售团队公司已经涵盖国内所有的省、自治区、直辖市,超过2500加三级医院,14000家二级医院或底级层医院及医疗机构。目前,公司拥有3378名营销人员,668名分销商以及2124第三方推广商组成的庞大销售及分销网络。
在生产上,公司共计拥有5个生产基地(位于杭州、沈阳、深圳、上海及意大利)。其中,公司共计拥有约3.8万升产能的单克隆抗体设施,在国内大分子制药公司中产能排第一;注射剂年产能9000万支(沈阳生产基地年产能5000万支,深圳生产基地年产能4000万支)。而意大利的生产基地,甚至可以为Mylan、UCB等企业提供CMO服务。
除了自主研发外,公司也在积极通过对外合作的方式,引入最新的产品与技术,从而与现有产品形成协同效应,增加核心治疗领域的产品组合。2020上半年,公司通过与阿斯利康、礼来、Toray、三星Bioepis、Refuge Biotechnologies、Vereau、TLC、Numab、GenSight、Sensorion及MPM等公司进行战略合作,提高公司整体的研发综合实力。
小结
在医改进入深水区之际,创新研发成为政策之下的主要逻辑。一方面,Big Pharma企业正在从仿创结合出发向创新药企转型,另一方面,新兴的Biotech企业则是凭借先进的技术在一些赛道开始创出一番天地。但无论是成熟药企还是新兴药企,我们可以观察到的是,近两年来“商业化进程”一词频出。换言之,创新研发,最终还是要落到实处,获批上市,看到销售业绩才是王者。
三生制药则是一个独特的存在。作为国内老牌的药企,核心产品拥有很强的技术壁垒,创新自主研发不说,还在不断地和外界深入合作取其精华。而在销售,生产环节,也是首屈一指,产、研、销的产业链完整,体系化竞争独具优势。
从资本市场来看,伴随着中报业绩密集发布时期,全国第三次集中采购也如约而至。相比起上半年医药板块一路高歌,近日走势的疲软与此次政策落地不无关系。但回看前两次的集中采购下的医药板块,常态化的带量采购已经让市场出现钝化,整体板块回撤也小很多。
对于三生制药而言,从今年3月到7月公司进行分拆三生国健上市,股价接连攀升,但随着第三次集采对于市场的影响,医药整体板块回撤,公司股价也随之回调。根据WIND数据显示,截止2020年8月24日收盘,公司PE为15.64倍,远低于公司近三年平均PE估值水平,处于明显低估。
从历史走势上来看,每一次政策性调整,例如全国集采,都是医药板块的“黄金坑”,每一次蛰伏也是为了更好的起跳。作为一家研发、销售、生产以及对外合作非常全面的药企,拥有体系化竞争的优势,在板块回调之际去关注,无疑是一个好的时机。
图表七:公司估值情况
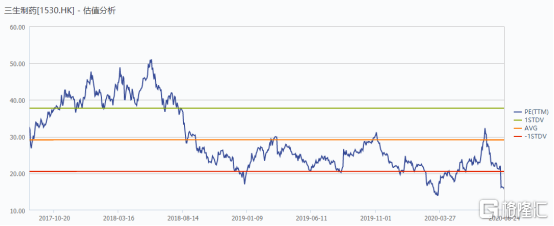
数据来源:WIND,整理